Nach zahlreichen Skandalen mit Medizinprodukten herrscht Unsicherheit bei Menschen, denen ein Operation bevorsteht. Die Durom-Selbsthilfegruppe (Durom-SHG) hat Informationen für Menschen zusammengestellt, die vor einer Hüft-TEP-Operation stehen.
Wann sollte operiert werden?
Wenn die Hüfte immer mehr schmerzt, die Beweglichkeit zunehmend eingeschränkt ist und das Laufen nur noch mit Mühe möglich ist, raten Ärzte in der Regel zu einer Hüft-TEP-Operation. Doch angesichts von mehr als 250.000 solcher Operationen jedes Jahr in Deutschland, ist Skepsis angesagt. Durch konservative Behandlungen wie Physiotherapie, Gymnastik und gesunde Ernährung kann ein OP-Termin oft mehrere Jahre hinaus geschoben werden. Und je später eine Hüft-TEP durchgeführt wird, um so besser für den Patienten.
Was passiert bei einer Hüft-TEP-OP?
Bei dieser wird die schadhafte und Schmerzen verursachende Hüfte ersetzt durch eine künstliche Hüfte aus Keramik, Metall, Porzellan oder eine Kombination der genannten. Bei einer Hüft-TEP, also eine Hüft-Totalendoprothesenoperation, wird der Kopf des Oberschenkelhalsknochens abgeschnitten. In die Öffnung wird ein Schaft eingetrieben und mit dem Knochen verkeilt (pressfit). Bei einer Metall-auf-Metall-Prothese (MoM) besteht der Schaft in der Regel aus einer Chrom-Kobalt-Titanlegierung.
Zementiert oder nicht zementiert?
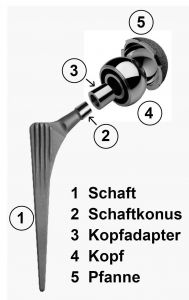
Bei zementfreien Hüft-TEPs wird der künstliche Schaft so weit mit Hammerschlägen in den Oberschenkelhalsknochen eingetrieben, bis er fest verkantet ist. Oben am Schaftende schaut ein Konus aus dem Oberschenkelhalsknochen heraus, auf welchen dann der Kugelkopf aufgesetzt wird. Das Gegenstück zum Kugelkopf, die Pfanne, wird im Becken eingepasst. Dazu wird der Beckenknochen ausgelasert bis die Kugel eingepasst werden kann. Zwischen Kugelkopf und Schaft wird bei einigen Modellen ein Zwischenstück eingesetzt, ein sogenannter Adapterkonus, der in unterschiedlichen Längen zur Verfügung steht. Dieser dient zum Ausgleich der Beinlänge und soll sicher stellen, dass auch nach der Hüft-TEP beide Beine gleich lang sind.
Ist das Knochenmaterial des Oberschenkelknochens zu porös, muss der Schaft in den Oberschenkelhalsknochen einzementiert werden. Danach ist ein Wechsel der Prothese wesentlich erschwert. Vorzuziehen ist bei einer Erst-Hüft-TEP deshalb stets die unzementierte Variante, wenn dies möglich ist.
Die Hüft-TEP-Operation im Trickfilm erklärt: Hier klicken
Eine genaue Beschreibung der Hüfte und ihrer Teile sowie weitergehende Informationen erhalten Sie, wenn Sie hier klicken.
Fragen an den Operateur vor einer OP
Um das Risiko einer fehlerhaften oder falschen Prothese gering zu halten, sollten vor der Operation mit dem Operateur folgende Fragen geklärt werden:
- Welches Prothesenmodell von welchem Hersteller soll implantiert werden?
- Aus welchem Material ist die Prothese?
- Wie lange ist das Prothesenmodell bereits auf dem Markt?
- Wie hoch ist die aktuelle Versagensquote bei diesem Modell?
- Wie lange ist die durchschnittliche Standzeit des Modells im Körper?
- Besteht bei Ihnen eine Materialallergie bzw. eine Allergie gegen das Material der Prothese?
- bei Neuentwicklungen („Innovationen“) nach klinischen Tests fragen.
- Tests und Funktionsprüfungen kritisch hinterfragen
- eher auf bewährte Modelle vertrauen, keine Experimente!
- Wie oft hat ihr Operateur das vorgeschlagene Modell bereits implantiert?
- Wie viele Re-Operationen hat der Operateur bisher bei dem vorgeschlagenen Modell durchgeführt?
- Welche Operationstechnik wird angewandt?
- Wie sieht es mit der Sterilität im OP aus?
Zweit- und/oder Drittmeinung einholen
Die Erfahrung zeigt, dass es wichtig ist, sich nicht auf die Aussagen und Empfehlungen eines Arztes oder Krankenhauses zu verlassen. Ärzte und Krankenhäuser empfehlen grundsätzlich die Methode, die sie routinemäßig anwenden. Auf die individuelle Befindlichkeit oder die körperlichen Voraussetzungen wird in der Regel nicht eingegangen. Deshalb sollte solange gesucht werden, bis man das Gefühl hat: „Jetzt passt es!“